「ピロリ菌を除菌したから、もう胃がんの心配はないだろう」と考えている方は少なくないかもしれません。しかし実際には、胃がんのリスクがゼロになるわけではありません。
ピロリ菌は日本人にとって非常に重要な感染症の一つであり、胃がんの発症に深く関わっていることが知られています。日本では2013年以降、ピロリ菌感染による胃炎に対して積極的に除菌治療が行われるようになりました。ただし、除菌による胃がん予防効果は「限定的」と報告されており、除菌後も長期的な観察が必要とされています。もちろん、除菌によって胃がんリスクを一定程度抑えることは可能なため、特に若い年代では早期の除菌が効果的と考えられています。
現在、胃がんの発症率は減少傾向にあるものの、がんによる死亡数では男性で2位、女性で4位を占めており、依然として警戒が必要な疾患です。年間約46,000人もの方が胃がんにより命を落としています。ピロリ菌除菌後も引き続き、胃カメラによる定期的な経過観察が重要とされています。今回は、ピロリ菌の除菌とその後の注意点について詳しく解説していきます。
目次
1章:ピロリ菌について医師が詳しく解説
1-1 ピロリ菌とは
ピロリ菌とは、正式名称を「ヘリコバクター・ピロリ(Helicobacter pylori)」といい、1983年にオーストラリアのワレン博士とマーシャル博士によって発見され、医学誌「ランセット」にて発表されました。
このピロリ菌は、主に乳幼児期に感染すると考えられており、感染経路の多くは家庭内、特に親から子への感染だとされています。ピロリ菌に感染すると胃の粘膜に慢性的な炎症を引き起こし、胃炎を発症するだけでなく、胃潰瘍や十二指腸潰瘍のリスクも高まります。また、胃過形成性ポリープや胃MALTリンパ腫との関連性も明らかになってきています。
1-2 ピロリ菌は胃がんリスクに直結する
胃がんのリスク要因としては、タバコ、アルコール、漬物の過剰摂取、遺伝的要素、発がん物質への曝露、ストレス、加齢などが知られています。しかし、その中でも特に注意すべき最大のリスクは「ピロリ菌感染」であると考えられています。
ピロリ菌と胃がんの関連性は非常に深く、世界保健機関(WHO)の外部組織である国際がん研究機関(IARC)も、ピロリ菌を胃がんの「確実な発がん要因」と認定しています。
日本人においては、ピロリ菌に感染していない人と比べると、感染者の胃がんリスクは15倍以上に高まると報告されています。つまり、ピロリ菌に感染しているだけで胃がんのリスクが飛躍的に高まるということです。実際、全胃がん患者の約8割はピロリ菌感染が関与しているとされています。
ピロリ菌が胃に定着すると、胃粘膜に持続的な炎症を引き起こします。この炎症が長期間続くことで、やがて胃がん発生の土台となるのです。そのため、ピロリ菌の除菌によって胃の炎症を鎮め、将来的な胃がんリスクを減少させることが非常に重要となります。
2章:ピロリ菌の除菌療法とは
2-1 1次除菌療法
ピロリ菌の除菌療法とは、薬剤を使用して胃内のピロリ菌を退治する治療方法です。一般的には、以下の①~③のお薬を7日間内服する「三剤併用療法」が行われます。これを「1次除菌」と呼びます。
【1次除菌療法の内容】
① PPI(プロトンポンプ阻害薬)またはP-CAB(カリウムイオン競合型アシッドブロッカー)
② AMPC(アモキシシリン)
③ CAM(クラリスロマイシン)
上記3種類のお薬を、1日2回、7日間服用します。
なお、1次除菌に失敗した場合には、「2次除菌療法」が行われます。2次除菌では、③CAMの代わりに別のお薬を用います。
2-2 2次除菌療法
【2次除菌療法の内容】
① PPIまたはP-CAB
② AMPC(アモキシシリン)
③ MNZ(メトロニダゾール)
日本では2013年2月より、ピロリ菌感染による慢性胃炎に対する除菌療法が健康保険の適用となり、多くの方が治療を受けています。
以前はPPIを使用した1次除菌により80~90%の高い除菌成功率が得られていましたが、近年ではクラリスロマイシン耐性菌の増加により成功率が60%程度に低下しています。これに対して、新薬であるP-CABを使用した除菌療法では、再び80~90%の高い除菌成功率が維持されているため、除菌治療ではP-CABの選択が推奨されています。
3章:ピロリ菌を除菌するとどうなる?
ピロリ菌を除菌することで、胃がんのリスクを低下させる効果が期待できます。
ただし、注意しなければならないのは、除菌によって胃がんリスクがゼロになるわけではないという点です。ピロリ除菌は胃潰瘍の再発予防には有効ですが、胃がんの発生そのものを完全に防ぐ効果については、まだ確固たるデータはありません。特に若い時期に除菌を行わなかった場合、十分な発がん予防効果が得られないことも指摘されています。
日本におけるピロリ菌感染率は現在20%台にまで低下している一方で、1970年代には70%以上の感染率を記録していました。胃がんによる年間死亡数は大きくは変わっていませんが、年齢調整死亡率は1985年の40%以上から2020年には20%強にまで半減しており、これは除菌療法の効果が一因と考えられています。
通常、ピロリ菌感染のない胃粘膜は、全体が淡いピンク色で滑らかな外観をしています。しかしピロリ菌に感染すると、胃粘膜に以下のような変化が生じます。
・襞(ひだ)の腫大
・びまん性発赤
・粘液の増加
・腸上皮化生
・胃粘膜萎縮
※すべての感染例で上記5つの所見が必ずしも見られるわけではありません。
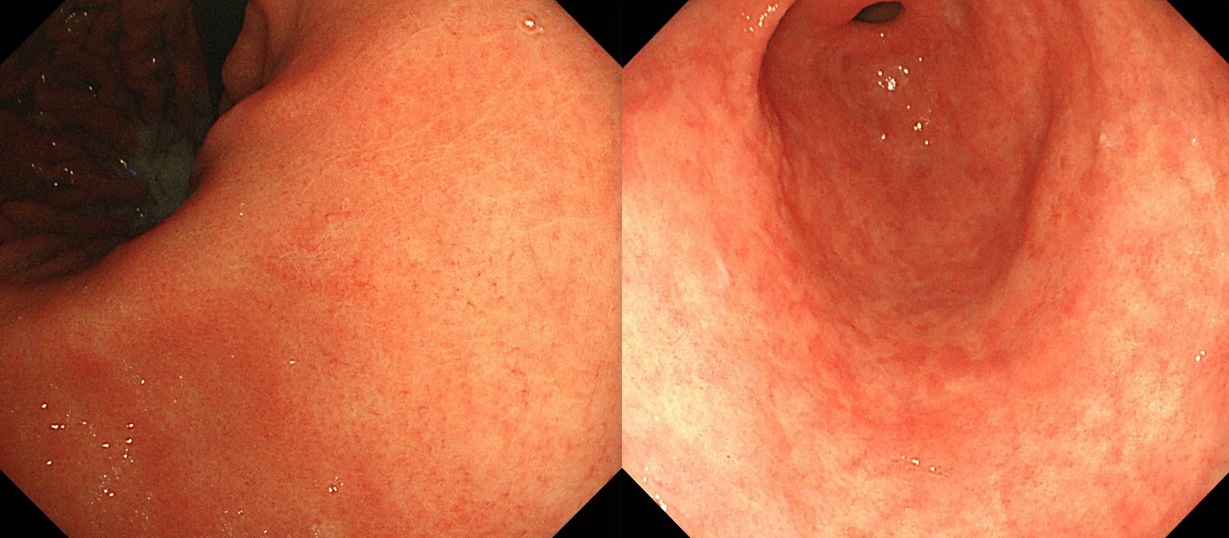
左:ピロリ菌未感染の胃粘膜 / 右:ピロリ菌感染の胃粘膜
左の未感染の胃粘膜は、全体が均一なピンク色で滑らかに見えます。一方、右のピロリ感染胃粘膜は、斑状に発赤が目立ち、粘膜が荒れた印象を受けることがわかります。
ピロリ菌除菌後には、上記5つの所見のうち、襞の腫大とびまん性発赤は改善することが多いですが、胃粘膜萎縮と腸上皮化生は残存する傾向があります。これらは除菌後も胃がんのリスク因子となるため、注意が必要です。
4章:ピロリ除菌後の胃の中はどう変わる?
かつて、強酸性の胃の中には細菌は生息できないと考えられていました。しかし、ピロリ菌の発見により、胃にも常在する細菌が存在することが明らかになりました。現在では、胃の中にも「胃内常在細菌叢(いないじょうざいさいきんそう)」と呼ばれる独自の細菌環境が存在することが知られています。
このような細菌群は「マイクロバイオータ(microbiota)」と呼ばれます。胃に存在するものは「胃内マイクロバイオータ」と呼ばれ、近年、メタゲノム解析という高度な遺伝子解析技術により研究が進められています。
現在わかっている主な胃内常在菌は以下の通りです。
・Firmicutes(ファーミキューテス門)
・Bacteroidetes(バクテロイデス門)
・Actinobacteria(アクチノバクテリア門)
・Proteobacteria(プロテオバクテリア門)
・Fusobacteria(フソバクテリア門)
健康な胃では、これらの菌がバランスよく共存していると考えられています。一方、ピロリ菌に感染した胃では、このバランスが崩れ、他の常在菌が減少し、細菌叢の多様性が低下することが報告されています。つまり、感染状態では胃内の細菌環境がピロリ菌に占拠され、他の細菌が住みにくくなっているのです。
また、ピロリ菌感染により慢性胃炎が進行すると、胃酸の分泌が低下して低酸状態になります。このような環境では、本来なら胃内に生息できない細菌が増殖しやすくなります。
近年、胃がん患者の胃内では、口腔内由来のStreptococcus(ストレプトコッカス属)やPrevotella(プレボテラ属)などの細菌が増加していることがわかっています。これらは低酸環境下で異常に増殖し、胃がん発生に関与している可能性が指摘されています。同様の現象は、大腸がん患者の腸内細菌叢でも観察されており、胃や腸の低酸環境が発がんリスクに影響している可能性が考えられています。
また、ピロリ除菌後に行われた研究では、平均2.55年の経過観察期間で、約10人に1人(約10%)に胃がんが発見されたという報告もあります。これは非常に高いリスクと考えられています。
一方で、以下の要素が胃がん発生リスクを低下させる可能性があると報告されています。
① 抗生物質の使用(ピロリ除菌以外の目的)
抗生物質の使用により、胃内や腸内のマイクロバイオータに変化が生じ、発がんリスクが低下している可能性が示唆されています。
② プロバイオティクス(善玉菌製剤)の使用
プロバイオティクスは、腸内細菌のバランス(ディスバイオーシス)を改善し、発がんリスクを低減させる可能性があると考えられています。プロバイオティクスに関しては、「腸活(健康的な食事・プロバイオティクス)で大腸がん予防」も参考にしてください。
今後、胃内や腸内のマイクロバイオータと胃がん発生の関連について、さらに詳しいメカニズム解明が期待されています。
5章:ピロリ除菌後でも胃がんリスクは残る
5-1 ピロリ菌を除菌しても安心できない理由
ピロリ菌除菌によって胃がんリスクは確かに低下しますが、リスクがゼロになるわけではありません。除菌後にも胃がんが発見されることは多く、長期的な経過観察が必要とされています。
除菌を行った場合でも、未感染者(ピロリ菌に感染したことがない人)に比べると、胃がん発症率は依然として高いことが知られています。つまり、除菌に成功しても、一定の割合で胃がんが発生するため、定期的な胃カメラ検査が不可欠なのです。
5-2 除菌後に胃がんリスクが高まる要因
特に以下のような条件を持つ方は、除菌後でも胃がんのリスクが高いとされています。
・男性
・高度な胃粘膜萎縮がみられる
・除菌前に胃がんの指摘を受けたことがある
・高齢者
これらに該当する方は、より慎重なフォローアップが求められます。
6章:ピロリ除菌後に発見される胃がんとは? 胃カメラの重要性
6-1 ピロリ除菌後胃がんとは
「ピロリ除菌後胃がん」とは、ピロリ菌除菌を終えた後に発見される胃がんを指します。
以前はピロリ菌感染状態で見つかる胃がんが主流でしたが、現在では、除菌後に発見される胃がんが多数を占めるようになっています。2013年以降、毎年およそ150万人が除菌治療を受けており、2025年時点では累計約1800万人以上が除菌を経験したと推計されています。
このため、今後も除菌後胃がんの発見例は増加すると考えられています。
6-2 ピロリ除菌後胃がんの難しさとは
ピロリ除菌後の胃がんは、通常の胃がんと比べて発見が難しい傾向にあります。
一般的に、除菌により胃粘膜のびまん性発赤(赤み)が改善するため、がんが見つかりやすくなると考えられていますが、実際には除菌後特有の変化により診断が困難になるケースが少なくありません。
ピロリ除菌後胃がんが発見しづらい主な理由は以下の通りです。
① 地図状発赤や斑状発赤などの特殊な胃炎が発生する
② ELA(低異型度上皮)が出現する
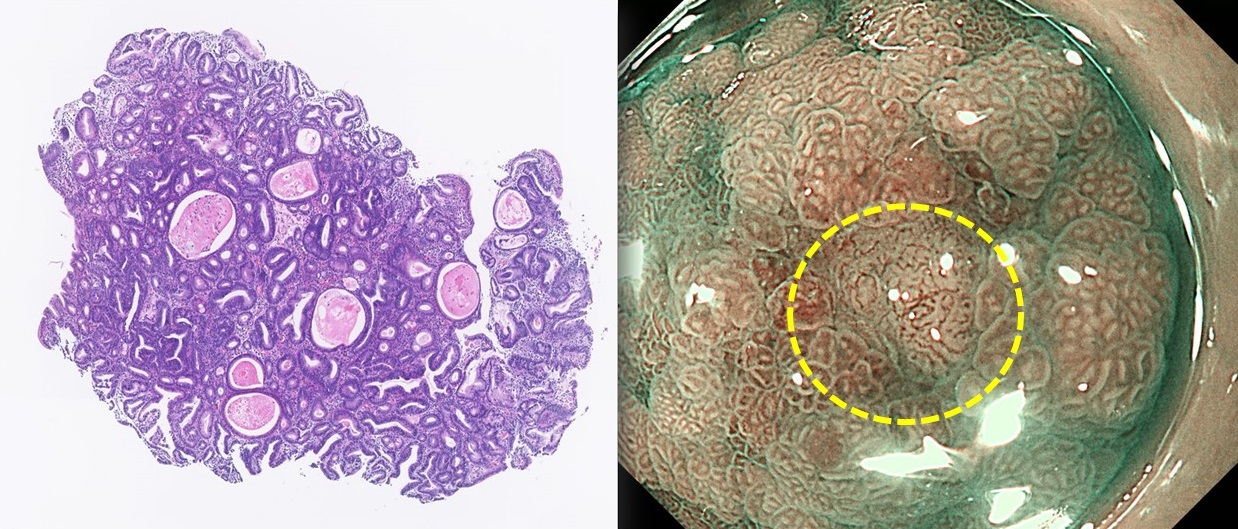
① 地図状発赤・斑状発赤とは?
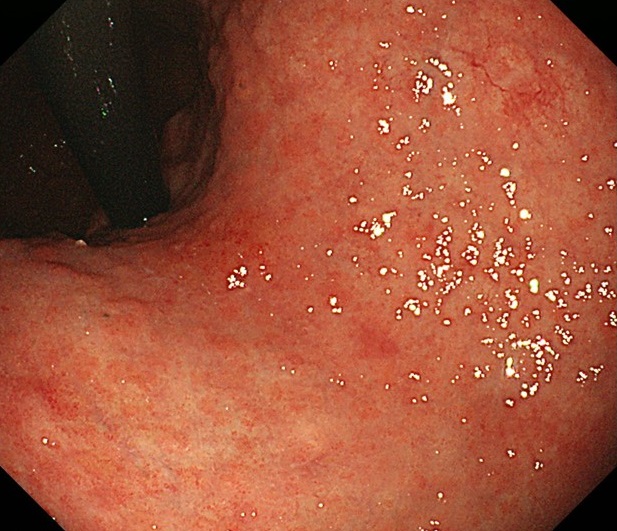
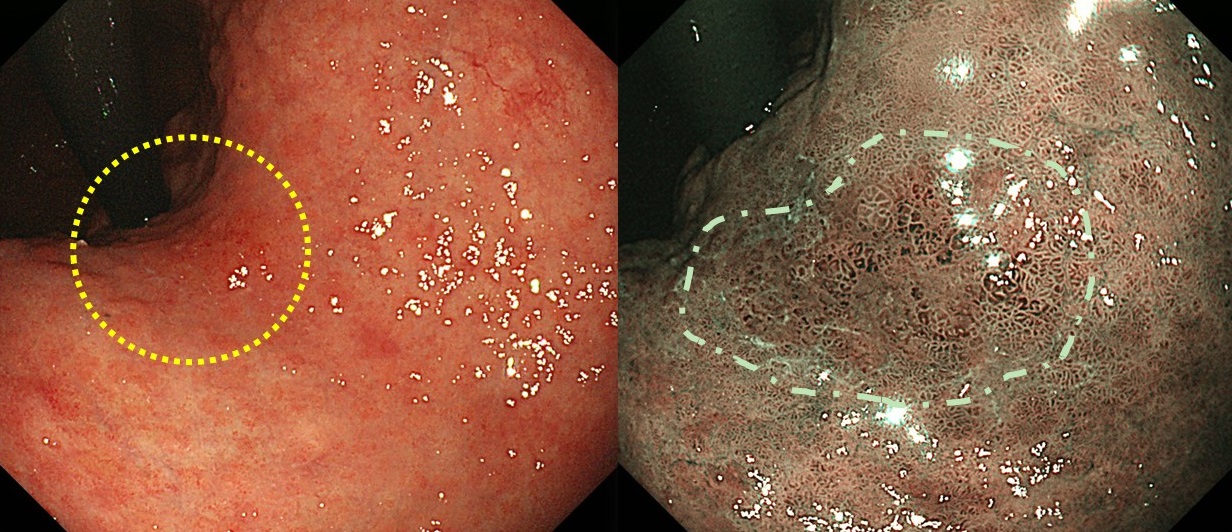
除菌後の胃粘膜には、不規則に広がる地図状発赤や斑状発赤が現れることがあります。この中に胃がんが発生するため、通常の胃炎との区別が非常に難しくなります。
上の写真にも、実は除菌後胃がんが隠れています。通常の内視鏡では見分けがつきにくいですが、NBI(Narrow Band Imaging:特殊波長観察)を用いることで、がん部位が濃いブラウン色に見えるようになります。
通常の内視鏡観察だけでは見逃しリスクが高く、除菌後の検査ではNBI観察を併用することが極めて重要です。当院でも除菌後胃カメラではNBIを活用し、見落としを防いでいます。
② ELA(低異型度上皮)とは?
ピロリ除菌後には、通常の胃炎に似た粘膜異常「ELA(epithelium with low-grade atypia)」が見られることがあります。このELAは見た目には普通の胃炎のように見えるため、がんとの区別が難しいことが特徴です。
さらに注意すべきは、ELAの下に本物の胃がんが潜んでいる場合があることです。
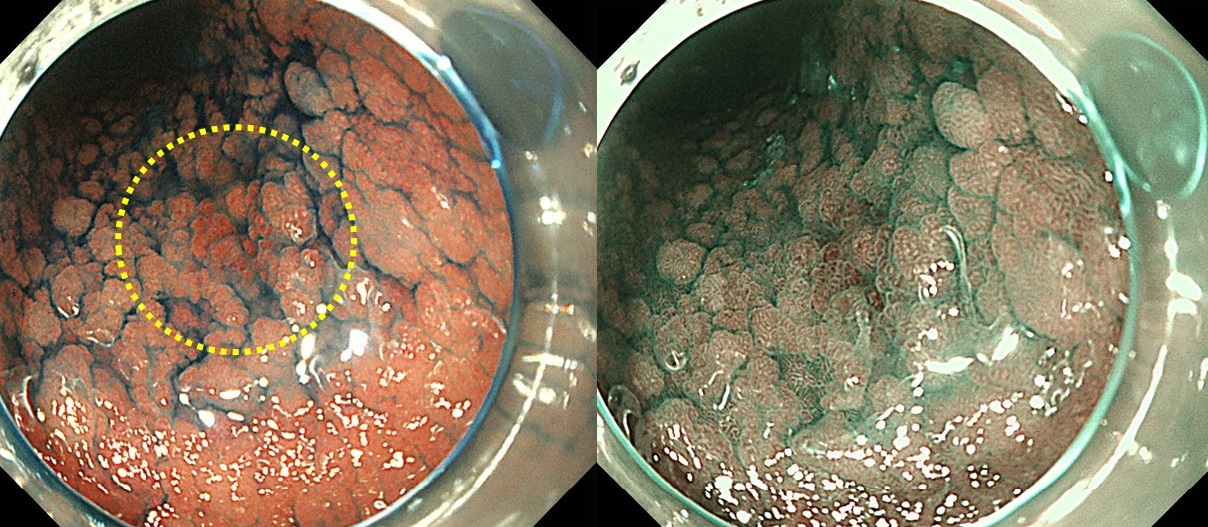
a(左):通常観察 / b(右):NBI観察
c(左):ELAの生検組織 / d(右):ELA剥がれ後に発見された胃がん
このように、ELAの存在を見逃さないこと、また定期的な再検査を行うことが極めて大切です。
6-3 ピロリ除菌後も、定期的な胃カメラ検査が必要
ピロリ除菌後の胃がんは、発見が難しいタイプが含まれるため、慎重な経過観察が不可欠です。
除菌後の胃がんは、進行すると粘膜下層に浸潤することもあり、発見が遅れると治療が難しくなる可能性があります。そのため、定期的な胃カメラ検査を受けることが重要です。
7章:ピロリ除菌後に胃カメラを受ける際の注意点
ピロリ菌除菌後も、一定の胃がんリスクは残るため、定期的な胃カメラ検査が推奨されます。
特に、除菌後の胃がんは発見が困難な場合があるため、以下のポイントに注意して検査を受けましょう。
① ピロリ除菌歴があることを、必ず問診時またはスタッフに伝える
② 除菌してから何年経過しているかを記載・報告する
③ 過去に胃がん治療を受けた経験があるかどうかを伝える
これらの情報を医療機関に伝えることで、より精度の高い内視鏡検査が受けられる可能性が高まります。
まとめ
ここまで、ピロリ菌除菌後の検査と、除菌後胃がんについて解説してきました。
重要なポイントを改めてまとめると、次のようになります。
・除菌後も定期的な胃カメラ検査が必要
・ピロリ菌以外の胃内常在菌の異常も胃がんリスクに関与している可能性がある
・男性、胃粘膜萎縮、胃がん既往歴、高齢といった条件は除菌後もリスク因子となる
・除菌後胃がんは発見が難しいケースが多いため、注意深い観察が不可欠
ピロリ菌を除菌した後こそ、より丁寧な経過観察と検査が必要になります。除菌後の定期的な胃カメラ検査を怠らず、専門医のフォローアップを受けましょう。
ピロリ除菌後の胃カメラ検査について不安がある方は、ぜひ専門外来にご相談ください。
※この記事は2022年8月25日に公開された内容を、2025年4月26日に最新の情報に基づき加筆・修正しました。
本記事の内容は、以下の文献・研究報告に基づいて構成しています。
・Uemura N, et al. Helicobacter pylori infection and the development of gastric cancer. N Engl J Med 2001; 345: 784-789.
・Take S, et al. The long-term risk of gastric cancer after the successful eradication of Helicobacter pylori. J Gastroenterol 2011; 46: 318-324.
・Noto JM, Peek RM Jr. The gastric microbiome, its interaction with Helicobacter pylori, and its potential role in the progression to stomach cancer. PLoS Pathog. 2017; 13: e1006573.
・Coker OO, et al. Mucosal microbiome dysbiosis in gastric carcinogenesis. Gut. 2018; 67: 1024-1032.
・Ferreira RM, et al. Gastric microbial community profiling reveals a dysbiotic cancer-associated microbiota. Gut. 2018; 67: 226-236.
・Sugimoto M, et al. Chemoprevention of gastric cancer development after Helicobacter pylori eradication therapy in an East Asian population: Meta-analysis. World J Gastroenterol 2020; 26:1820-1840.
・Tsuda M, et al. Effect on Helicobacter pylori eradication therapy against gastric cancer in Japan. Helicobacter 2017; 22: e12415.
・Arai J, et al. Use of Antibiotics and Probiotics Reduces the Risk of Metachronous Gastric Cancer after Endoscopic Resection. Biology 2021; 10: 455.
・Kitamura Y, et al. Characteristic epithelium with low-grade atypia appears on the surface of gastric cancer after successful Helicobacter pylori eradication therapy. Helicobacter 2014; 19: 289-295.
施設紹介
東京千住・胃と大腸の消化器内視鏡クリニック 足立区院 >>
ホームページ https://www.senju-ge.jp/
電話番号 03-3882-7149
住所 東京都足立区千住3-74 第2白亜ビル1階
| 診療時間 | 月 | 火 | 水 | 木 | 金 | 土 | 日 |
|---|---|---|---|---|---|---|---|
| 9:00~12:00 | ● | ● | ● | ● | ● | ● | ● |
| 14:00~17:30 | ● | ● | ● | ● | ● | ● | ※ |
※予約検査のみ
※祝日のみ休診
JR北千住駅西口より徒歩2分、つくばエクスプレス北千住駅より徒歩2分、東京メトロ日比谷線北千住駅より徒歩2分、東京メトロ千代田線北千住駅より徒歩2分、東武伊勢崎線北千住駅より徒歩3分