「前にもあったけど、また便に血が混じっている…これって大丈夫なのかな?」
こんな経験はありませんか?若い方で血便が続く場合、潰瘍性大腸炎という病気の可能性があります。潰瘍性大腸炎は、大腸の粘膜にびらんや潰瘍ができる炎症性腸疾患(IBD)の一種で、慢性的に経過する疾患です。
この病気は10代後半から30代前半の発症が多く、日本では現在、22万人以上の患者がいるとされています。主な症状には腹痛、下痢、そして血便があり、症状が良くなったり悪くなったり(寛解と再燃)を繰り返しながら進行するため、日常生活への影響が大きい疾患です。
診断には、潰瘍性大腸炎に特有の症状の確認に加え、大腸カメラで大腸粘膜を直接観察することが必要です。検査を通じて炎症の程度や治療の効果を把握し、また大腸がんのリスクを考慮して、必要に応じて定期的な内視鏡検査を行うことも推奨されます。
今回は「潰瘍性大腸炎」について、大腸カメラを受ける意義も含め、詳しく解説していきます。
潰瘍性大腸炎は、日本国内で22万人以上の患者がいるとされ、米国に次いで世界で2番目に患者数が多い国といわれています。この病気は完治が難しく、長期的に症状が続く慢性疾患です。日本では「指定難病」にも認定されており、治療の目標は以下の2つです。
・症状の緩和(短期的目標)
・予後の改善(長期的目標)
この2つの目標を達成することが、潰瘍性大腸炎の治療において重要です。
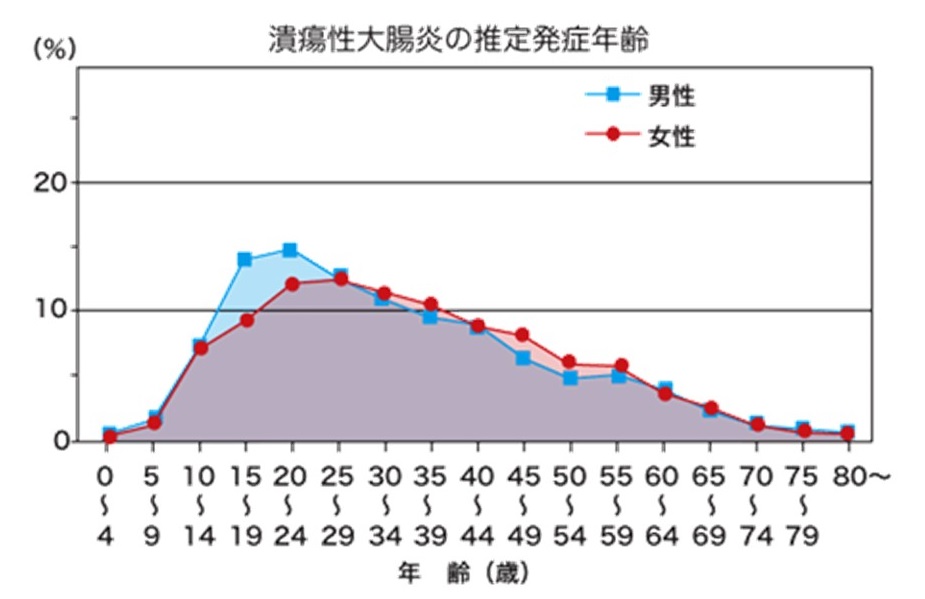
1-1、潰瘍性大腸炎の発症年齢
潰瘍性大腸炎は、特に10代後半から30代前半にかけて多く発症し、男女差では男性の方がやや若年での発症が多いとされています。
発症年齢のピーク
・男性:20~24歳
・女性:25~29歳
若年層に多い病気ではありますが、高齢者での発症も珍しくありません。さらに、長期間の経過をたどる病気であるため、現在は高齢の潰瘍性大腸炎患者の数も増加傾向にあります。
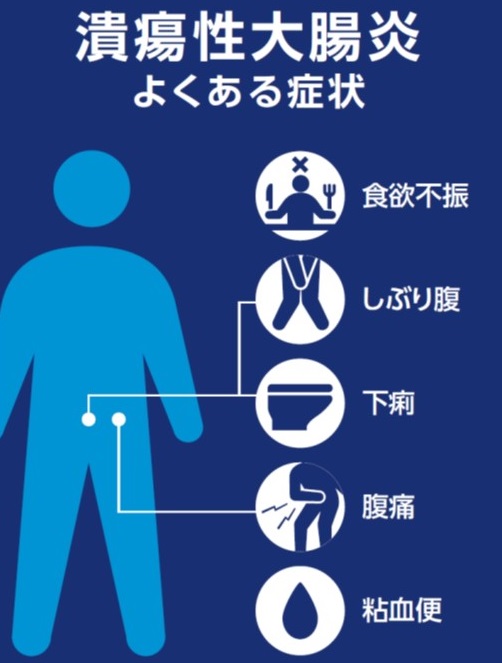
1-2、潰瘍性大腸炎の症状
その他、以下のような症状が見られることがあります。
- 粘血便(粘液と血液が混ざった便)
- 下痢
- 血性下痢
特に病状が進行すると、粘液や血液が混ざった便や、頻回の血性下痢が現れることがあります。
また、以下のような全身症状がみられる場合もあります。
- 腹痛
- 発熱
- 食欲不振
- 貧血
- 体重減少
血便の有無が診断の目安となりますが、繰り返す腹痛や下痢などがある場合にも潰瘍性大腸炎の可能性があるため注意が必要です。
10代・20代で血便を繰り返している方は、早めに専門の医療機関を受診しましょう。
1-3、潰瘍性大腸炎の原因
潰瘍性大腸炎の明確な原因は、いまだ解明されていません。
現在、発症に関与していると考えられている要因には以下のようなものがあります。
① 遺伝的な素因
潰瘍性大腸炎は、家族内での発症報告があることから、遺伝的要因が関与していると考えられています。最近では発症に関係する複数の遺伝子も明らかになっていますが、遺伝子だけで発症するわけではなく、生活習慣や腸内環境など複数の因子が関係しているとされています。
② 環境因子(食生活・感染・衛生環境など)
先進国を中心に患者数が多い一方で、発展途上国では少ないとされています。しかし近年では、東南アジアやアフリカ諸国でも患者数が増えており、工業化や食生活の欧米化、衛生環境の変化が影響していると考えられています。
③ 腸内細菌の異常(Dysbiosis)
潰瘍性大腸炎の患者では、腸内細菌のバランスが崩れた「ディスバイオーシス」の状態にあることが知られています。善玉菌と悪玉菌のバランスが乱れることで腸内環境が悪化し、腸粘膜に炎症を引き起こす可能性があります。ただし、炎症が原因でディスバイオーシスになるのか、逆にディスバイオーシスが炎症を引き起こすのかは、まだ研究段階です。
*腸内細菌とディスバイオーシスについて詳しくは、関連コラム「大腸がん予防には腸活(健康的な食事・プロバイオティクス)が有効!」もご覧ください。
1-4、潰瘍性大腸炎は大腸がんのハイリスクのご病気
潰瘍性大腸炎は、大腸がんのリスクが高いことが知られており、定期的な大腸カメラ(内視鏡検査)が推奨されます。
特に、潰瘍性大腸炎の長期罹患者に発生する大腸がんは、潰瘍性大腸炎関連大腸がん(Colitis-associated cancer:CAC)と呼ばれ、通常の大腸がんとは異なる経過をたどることがあります。
発症後10年で約3.3%、20年で約12.1%の割合でがんや前がん病変(Dysplasia:異形成)が確認されるという報告もあり、こうした背景から、外科的治療の対象となる患者さんも増加しています。
各国のガイドライン(日本を含む)では、発症から8年以上経過した方を対象に、サーベイランス内視鏡として定期的な大腸カメラの実施が推奨されています。ただし、8年未満の症例でもがんの報告例があるため、検査の頻度やタイミングについては専門医と相談しながら決めることが大切です。
大腸がんを早期に発見し、重症化を防ぐためにも、適切な時期と間隔での内視鏡検査が極めて重要です。
2章、潰瘍性大腸炎の検査
潰瘍性大腸炎が疑われた場合には、主に大腸カメラ(内視鏡検査)と血液検査が行われます。それぞれの目的や重要性について解説していきます。
大腸カメラについて、もっとわかりやすく知りたい方は、こちらのマンガをご覧ください。
2-1、大腸カメラ(大腸内視鏡検査)
潰瘍性大腸炎の診断には、大腸カメラによる大腸粘膜の直接観察が必要不可欠です。大腸カメラを実施する理由は、主に次の2点に集約されます。
① 潰瘍性大腸炎の確定診断のため
潰瘍性大腸炎かどうかを判断するには、内視鏡で粘膜の状態を直接確認する必要があります。大腸は直腸から盲腸まで約1.5メートルの長さがあり、炎症がどの部位にあるかを見極めることが重要です。
また、似た症状を呈する別の病気(感染性腸炎や虚血性腸炎など)との鑑別のためにも、大腸カメラによる詳細な観察が必要です。必要に応じて、粘膜から組織を採取し、病理検査に回すこともあります。
基本的には、大腸全体の観察が望まれますが、症状が強く出ている活動期には前処置(下剤)を使用せず、可能な範囲で観察することもあります。活動期には固形の便が少ないため、前処置なしでも観察が可能な場合もあります。
② 潰瘍性大腸炎の重症度を評価するため
診断だけでなく、炎症の程度を把握することも大腸カメラの重要な役割です。以下のような内視鏡所見をもとに、潰瘍性大腸炎の重症度を評価します。
- 血管透見消失:健康な粘膜では血管が透けて見えますが、炎症があると血管像が不明瞭になります。
- 粘膜粗造・顆粒状:正常な粘膜は滑らかですが、炎症が続くと表面が荒れてきます。
- びらん・潰瘍:炎症が進行すると粘膜にびらんや潰瘍が見られます。
- 易出血性:炎症で粘膜がもろくなり、触れるだけで出血する状態です。
これらの所見を総合的に評価し、「UCEIS(Ulcerative Colitis Endoscopic Index of Severity)」というスコアで重症度を判定します。UCEISは、内視鏡所見と患者の症状との相関が高く、治療方針の決定にも役立ちます。
UCEISスコア(簡易版)
| 評価項目 | スケール | 定義 |
|---|---|---|
| 血管像(V) | 正常(0) | 血管が明瞭に見える |
| 斑状消失(1) | 一部の血管像が不明瞭 | |
| 消失(2) | 血管像が完全に消失 | |
| 易出血性(B) | なし(0) | 出血は見られない |
| 粘膜出血(1) | 点状や縞状の出血 | |
| 軽度出血(2) | 液状の出血が確認される | |
| 中~重度出血(3) | 明らかな湧出性出血 | |
| 粘膜損傷(U) | なし(0) | 正常な粘膜 |
| びらん(1) | 小さな浅い粘膜欠損 | |
| 表面潰瘍(2) | 5mm以上の粘膜欠損 | |
| 深掘れ潰瘍(3) | 深くえぐれた潰瘍 |
このように、大腸カメラは潰瘍性大腸炎の診断と重症度評価の両面で非常に重要な検査です。
2-2、潰瘍性大腸炎のバイオマーカー(治療効果の指標)
潰瘍性大腸炎の診断には大腸カメラが必須ですが、治療の効果を確認するために毎回内視鏡を行うのは、身体的にも負担がかかります。そこで、内視鏡の代わりに治療効果を判定するための「バイオマーカー」が活用されます。
潰瘍性大腸炎で利用される代表的なバイオマーカーには、以下の2つがあります。
① 便中カルプロテクチン
便中カルプロテクチンは、便の中に含まれる好中球由来のたんぱく質であり、腸管内での炎症の度合いを反映します。検査は便を提出するだけなので簡便で、患者の負担が少ないのが特徴です。
潰瘍性大腸炎の活動性を評価する補助的な検査として有用ですが、カルプロテクチンは他の疾患(感染性腸炎、NSAIDsの使用など)や個人の体質・年齢・肥満などの影響も受けるため、総合的に判断する必要があります。
② 血清LRG(Leucine-rich alpha-2 glycoprotein)
血清LRGは、潰瘍性大腸炎の新しい炎症マーカーの一つです。活動性が高まると血中のLRG濃度も上昇するため、血液検査で病勢をモニタリングする手段として注目されています。
ただし、リウマチ性疾患や感染症、悪性腫瘍など他の炎症性疾患でもLRGが高くなることがあるため、検査結果は医師による総合的な判断が必要です。
2-3、その他の血液検査や画像検査
潰瘍性大腸炎では、内視鏡検査やバイオマーカーに加えて、他の検査を併用して全身状態や病状の把握を行います。
① 採血検査
炎症の有無や程度を把握するために、CRP(C反応性タンパク)、白血球数、赤沈(赤血球沈降速度)などを測定します。
また、血便による貧血の有無を確認するためにHb(ヘモグロビン)や血清鉄の測定も行われます。栄養状態の評価としては、総蛋白やアルブミンの値が参考になります。
さらに、肝機能・腎機能など他臓器への影響がないかも併せて確認します。
② CT検査・MRI検査
これらの画像検査では、腸管の炎症状態だけでなく、合併症の有無や他臓器の異常も調べることが可能です。特に以下のような腸管外合併症の評価に有用です。
- 原発性硬化性胆管炎
- 強直性脊椎炎
- 骨粗しょう症
- 尿路結石症
腸管だけでなく、関連する全身の状態を把握する上で、CT・MRI検査は重要な役割を果たします。
③ 腹部エコー検査
腹部エコーでは、腸管の浮腫(むくみ)や拡張の程度をリアルタイムで観察することができます。また、胆管や腎臓など腸管外合併症のチェックにも活用されます。
ただし、腸管にガスが多い場合は画像が不明瞭になることがあるため、検査結果の解釈には注意が必要です。
3章、潰瘍性大腸炎の治療
潰瘍性大腸炎の治療は、かつては主に症状を抑えることが目的でしたが、近年では「粘膜治癒」を目指した治療が主流となっています。つまり、見た目にも正常な状態の大腸粘膜を回復させることが治療のゴールとなってきました。
3-1、5-ASA製剤
5-ASA(5-アミノサリチル酸)製剤は、潰瘍性大腸炎の治療における第一選択薬(First Line Drug)です。40年以上の使用実績があり、有効性と安全性の高さが確立されています。
5-ASA製剤の主成分であるメサラジンには、炎症を引き起こす化学伝達物質(ロイコトリエンなど)の生成を抑える働きがあります。これにより、腸管粘膜の炎症を鎮める作用を持っています。
ただし、メサラジンは小腸で吸収されやすいため、大腸に届けるためには薬剤に特殊な加工(DDS:ドラッグ・デリバリー・システム)が施されています。各製剤によって、このメサラジンの運搬方法が異なっています。
現在、日本で使用可能な5-ASA製剤には以下のものがあります。
- ① サラゾピリン®(サラゾスルファピリジン)
- ② ペンタサ®(メサラジン徐放錠)
- ③ アサコール®(メサラジン腸溶錠)
- ④ リアルダ®(メサラジン腸溶錠)
①のサラゾピリン®はスルファピリジンとメサラジンの複合薬である一方、②~④はメサラジン単剤です。それぞれの特徴を見ていきましょう。
① サラゾピリン®
サラゾピリン®は腸内細菌によって分解され、スルファピリジンとメサラジンに分かれます。このうち、メサラジンが大腸の粘膜で炎症を抑えます。
副作用は主に以下の通りです:
- アレルギー反応
- 消化器症状(下痢・腹痛・膨満感)
- 可逆性の精子減少
- 頭痛
これらの多くはスルファピリジンに起因します。メサラジン単剤にも以下のような副作用があります:
- 消化器症状
- 無顆粒球症
- 血小板減少
- 心筋炎
- 肝障害
そのため、内服中は定期的に採血を行い、異常がないか確認する必要があります。
② ペンタサ®
ペンタサ®は、エチルセルロースという物質でコーティングされており、小腸の上部(空腸)からメサラジンが放出されます。そのため、大腸での効果がやや不十分になることもあります。
一方で、腸の広範囲に有効成分が届くため、小腸にも病変が及ぶクローン病の治療には適しているとされています。
③ アサコール®
アサコール®は、pHに反応する特殊コーティングを採用しています。pHが6.8〜7.0以上になるとコーティングが溶け、メサラジンが放出される仕組みです。
この仕組みにより、回腸末端〜大腸にかけてしっかりと薬効を発揮できる設計となっており、S状結腸での薬剤濃度も高いと報告されています。
④ リアルダ®
リアルダ®は、さらに進化した「MMX(マルチ・マトリックス・システム)」という構造を採用しており、親水性と親油性の素材を組み合わせることでメサラジンを大腸内にゆっくりと持続的に放出します。
この持続的放出により、リアルダ®は腸内全体に均等に薬が行き届きやすい設計となっています。
製剤選択のポイント
5-ASA製剤には飲み薬だけでなく、注腸剤や顆粒剤などもあります。新しい薬が必ずしも良いというわけではなく、それぞれの患者さんに適した製剤を選ぶことが重要です。
また、pH依存型の薬剤(アサコール®やリアルダ®)では、薬が溶けずにそのまま排泄されてしまうケースもあります。実際、内視鏡検査で溶けていない薬剤が大腸内に見られることがあります。
報告によっては、約10%以上の薬が未溶解のまま排泄されているとの指摘もあり、その場合は薬の効果が十分に発揮されていないことになります。
潰瘍性大腸炎の約3分の2は、高用量の5-ASA製剤や局所製剤の適切な併用によって、安定した経過を得ることができます。そのため、自分に合った製剤を使用し、薬がしっかり患部に届いているかを確認しながら治療を継続することが大切です。
3-2、ステロイド
ステロイドは、1950年代から炎症性腸疾患に使用されてきた歴史ある治療薬です。潰瘍性大腸炎の第一選択薬は5-ASA製剤ですが、それで効果が得られない場合には、ステロイドが第二選択薬(Second Line Drug)として使用されます。
中等症以上の潰瘍性大腸炎では、ステロイド治療が必要になるケースが多く、患者さんの病状に応じて、適切な種類・量のステロイド薬が選ばれます。かつては長期間にわたる投与や繰り返しの使用で副作用が問題となっていましたが、近年ではより副作用が少なく、局所的に効果を発揮する新しい製剤も登場しています。
潰瘍性大腸炎で使用される主なステロイド製剤には、以下のような種類があります。
- 経口プレドニゾロン
- 静注プレドニゾロン
- ブデソニド注腸フォーム(レクタブル®注腸フォーム)
- プレドネマ®注腸
- リンデロン®坐剤
- ステロネマ®注腸
通常は、まず局所的に作用する注腸製剤から使用し、症状が重い場合には経口投与や点滴による静脈注射が選択されます。
ステロイドの使用量の目安
- 中等症例:経口プレドニゾロン 30〜40mg/日
- 重症例:静注プレドニゾロン 40〜80mg/日(入院管理)
効果が現れたら、徐々に減量していき、原則として3ヶ月以内にステロイドから離脱することが推奨されます。
ステロイドの主な副作用
- 白内障・緑内障
- 糖代謝異常(耐糖能異常)
- 骨粗しょう症
- 感染症への抵抗力低下(易感染性)
- 副腎皮質機能抑制
これらの副作用を考慮しながらも、症状が強い場合にはステロイドの使用が必要不可欠です。使用期間や用量については、必ず専門医と相談の上で調整することが重要です。
特に高齢者では、骨密度の低下を予防するためにビスホスホネート製剤などを併用することも検討されます。
近年では、ステロイドを使用しない「ステロイドフリーの寛解維持」を目指す治療が現実的な目標となりつつあります。
3-3、免疫調整薬
潰瘍性大腸炎に使用される免疫調整薬には、以下の2つがあります。
- イムラン®(アザチオプリン)
- ロイケリン®(6-メルカプトプリン)※保険適応外
これらは、特に「ステロイド依存型」の潰瘍性大腸炎において、ステロイドの使用量を減らす(または中止する)目的で使用されます。
免疫調整薬は、過剰な免疫反応を抑えることで病状の安定化を図り、寛解状態を維持するための治療薬です。
主な副作用
- 白血球減少症・骨髄抑制
- 易感染性
- 全身脱毛
- 肝障害
これらの重篤な副作用のリスクがあるため、以前は使用が難しいとされていました。しかし近年では、「NUDT15遺伝子」の検査により、副作用の出やすさを事前に判別できるようになり、より安全な使用が可能となっています。
免疫調整薬の使用に際しては、定期的な血液検査などのモニタリングが欠かせません。
3-4、免疫抑制薬
免疫抑制薬は、免疫細胞の働きを抑えることで潰瘍性大腸炎の炎症をコントロールする薬剤です。特に中等症から重症の患者さんに対して使用されることがあります。
代表的な免疫抑制薬には、以下のものがあります。
- プログラフ®(タクロリムス)
- ネオーラル®(シクロスポリン)※保険適応外
これらの薬は、T細胞という免疫細胞の活性化を抑制し、腸管の炎症を鎮める作用があります。ただし、免疫を抑える作用が強いため、感染症(特にニューモシスチス肺炎など)には注意が必要です。ステロイドとの併用時には特にリスクが高まるため、十分な感染対策が求められます。
また、副作用として以下のようなものが報告されています:
- シクロスポリン:多毛症、歯肉肥厚
- タクロリムス:腎機能障害、電解質異常
さらに、グレープフルーツジュースはタクロリムスの血中濃度を上昇させるため、併用は禁止されています。服用中は食事・飲料にも注意が必要です。
3-5、生物学的製剤
潰瘍性大腸炎に対する治療は、この20年間で大きく進化しました。特に、生物学的製剤の登場により、これまで手術が必要だったような重症例でも、内科的にコントロールが可能となってきています。
生物学的製剤は、体内で炎症を引き起こす原因物質(サイトカインなど)に直接作用して、過剰な免疫反応を抑える薬です。いずれも注射や点滴によって体内に投与されます。
潰瘍性大腸炎で使用される代表的な生物学的製剤には、以下のような薬があります。
- レミケード®(インフリキシマブ)
- ヒュミラ®(アダリムマブ)
- シンポニー®(ゴリムマブ)
- エンタイビオ®(ベドリズマブ)
- ステラーラ®(ウステキヌマブ)
これらは、いずれも難治性潰瘍性大腸炎に対して承認されており、患者さんの状態や既存の治療との相性を見ながら選択されます。
生物学的製剤により、症状のコントロールだけでなく、粘膜の治癒や長期的な寛解の維持が期待できます。近い将来、患者さん一人ひとりに合った「オーダーメイド医療」への応用も視野に入っています。
3-6、JAK阻害薬
JAK阻害薬は、潰瘍性大腸炎の炎症反応を抑制する新しいタイプの内服薬です。炎症を引き起こすサイトカインの情報伝達経路(JAK-STAT経路)をブロックすることで、免疫反応をコントロールします。
JAK阻害薬は、特に中等症〜重症の潰瘍性大腸炎で、他の治療で効果が得られなかった場合に使用されます。
現在、潰瘍性大腸炎で使用されるJAK阻害薬には以下のようなものがあります。
- ゼルヤンツ®(トファシチニブ)
- ジセレカ®(フィルゴチニブ)
いずれも経口薬であるため、通院・注射の負担が軽く、患者さんのQOL(生活の質)向上に寄与します。一方で、感染症のリスクや血栓症の報告もあるため、使用には慎重な判断と定期的なモニタリングが必要です。
3-7、血球成分除去療法
血球成分除去療法(G-CAP、L-CAP)は、日本で開発された治療法で、5-ASA製剤やステロイドなどで効果が不十分な場合に選択されることがあります。
この治療法では、人工透析に似た装置を使用して血液を一時的に体外に取り出し、炎症に関与する白血球(顆粒球・単球・活性化リンパ球など)を除去した後、再び体内へ戻します。これにより、腸粘膜の炎症を軽減することができます。
血球成分除去療法には主に2つの種類があります。
① G-CAP(顆粒球除去療法)
酢酸セルロースビーズを使用した専用のカラムにより、主に顆粒球と単球を選択的に除去します。除去率はL-CAPに劣りますが、治療効果は同等とされています。
② L-CAP(白血球除去療法)
ポリエステル不織布を使用し、顆粒球・単球に加えてリンパ球や血小板も除去できる治療法です。より広範な白血球除去が可能で、炎症の抑制効果が期待されます。
いずれの方法も、薬剤による副作用が少なく、安全性が高いという利点がありますが、治療には専用の装置と医療スタッフの管理が必要です。
4章、潰瘍性大腸炎についてのQ&A
Q1、食事はどんなものを食べてはいけないのですか?
症状が落ち着いている「寛解期」には、極端な食事制限は必要ありません。ただし、普段からなるべく腸に優しい食事を心がけ、消化に悪いものや刺激の強い食品は控えるようにしましょう。
特に以下の食品は注意が必要です:
- 脂肪分の多い食品(揚げ物、菓子、ナッツ類など)
- 繊維の多い食品(イモ類、こんにゃく、野菜、きのこ、海藻など)
- 消化に悪い食品(貝類、イカ、エビなど)
- 刺激物(唐辛子、香辛料など)
- 脂肪分の多い乳製品(チーズ、生クリーム、アイスなど)
ただし、これらをすべて避ける必要はありません。人によって合う・合わない食べ物が異なるため、自分の体調と相談しながら、慎重に見極めていくことが大切です。
野菜類に関しては、加熱して柔らかくすることで負担が軽くなります。生野菜よりも煮物やスープなどにして摂取するのが望ましいでしょう。
Q2、潰瘍性大腸炎はストレスで悪化しますか?
潰瘍性大腸炎の診療において、精神的ストレスが重視されることは少ないものの、心理的な要因が発症や再燃に関係するという報告は数多くあります。
近年の研究では、精神的ストレスが腸内細菌叢(腸内フローラ)のバランスに影響を与えることが明らかになってきています。このバランスが乱れた状態を「ディスバイオーシス(Dysbiosis)」と呼びます。
ディスバイオーシスが進行すると、発がん、慢性炎症、うつ病、動脈硬化など、さまざまな悪影響が報告されており、潰瘍性大腸炎の病態にも関与している可能性が示唆されています。
そのため、ストレスをため込まない生活習慣や心のケアも、潰瘍性大腸炎の再燃予防や症状の安定に役立つと考えられています。
Q3、治療の期間はどのようになっていますか?
潰瘍性大腸炎の治療期間は、個人の症状や経過によって異なります。潰瘍性大腸炎は慢性の病気であり、一度診断されると長期的に付き合っていく必要があるご病気です。
潰瘍性大腸炎の経過は、症状のある「活動期」と、症状が落ち着いた「寛解期」を繰り返すのが特徴です。
寛解期には、症状がなくても5-ASA製剤などの内服を継続することがとても大切です。薬の服用を自己判断で中止すると、再発のリスクが高まります。
再燃した場合には、5-ASA製剤の増量や、ステロイド、免疫調整薬、生物学的製剤などの追加治療が必要になることもあります。
継続的な治療と定期的な診察によって、寛解状態を長く維持することができます。
Q4、費用はどのようになっていますか?
潰瘍性大腸炎は「指定難病」に該当する病気であり、中等症以上と診断された方は、医療費助成制度の対象になります。
この「難病医療助成制度」では、1ヶ月あたりの医療費に上限が設定されており、それを超えた分は公費で補助される仕組みとなっています。
指定特定医療における月額自己負担限度額
| 階層区分 | 階層の基準 | 一般 | 高額かつ長期 | 人工呼吸器等装着者 | |
|---|---|---|---|---|---|
| 生活保護 | ー | 0 | 0 | 0 | |
| 低所得Ⅰ | 非課税(世帯) | 本人年収 ~80万円 | 2,500 | 2,500 | 1,000 |
| 低所得Ⅱ | 本人年収 80万円超~ | 5,000 | 5,000 | ||
| 一般所得Ⅰ | 課税世帯(7.1万円未満) | 10,000 | 5,000 | ||
| 一般所得Ⅱ | 課税世帯(7.1万円以上〜25.1万円未満) | 20,000 | 10,000 | ||
| 上位所得 | 課税世帯(25.1万円以上) | 30,000 | 20,000 | ||
※「難病の患者に対する医療等に関する法律施行令」より引用
※医療費助成制度は今後変更となる可能性があります。最新情報は厚生労働省の公式サイト等をご確認ください。
潰瘍性大腸炎の治療は、継続と安心が何より大切です。
当院では、プライバシーに配慮した診療体制も整えています。
まとめ
今回は、潰瘍性大腸炎について解説しました。
潰瘍性大腸炎が疑われる方は、以下のポイントを意識することが重要です。
- 潰瘍性大腸炎は若い方に多い慢性疾患
- 血便が続く場合は、早めに専門外来を受診する
- 診断には大腸カメラ(内視鏡検査)が必要
- 潰瘍性大腸炎の長期罹患は大腸がんのリスクが高まる
潰瘍性大腸炎は、長期的な経過をたどる病気です。一度診断されたら、定期的な診察と検査、適切な治療を継続することが重要となります。
治療方法も以前に比べて多様化しており、患者さん一人ひとりに合った治療選択ができる時代になっています。気になる症状がある場合は、早めに専門の医療機関にご相談ください。
参考文献・関連リンク
- Hata K, et al. Surveillance Colonoscopy for Ulcerative Colitis. Am J Gastroenterol 2019; 114: 483-489.
- Eaden J, et al. Grading Dysplasia in Ulcerative Colitis. J Pathol 2001; 194: 152-157.
- Eluri S, et al. Undetected Colorectal Cancer in IBD. Dig Dis Sci 2017; 62: 3586-3593.
- Olén O, et al. Colorectal Cancer in Ulcerative Colitis: A Scandinavian Study. Lancet 2020; 395: 123-131.
- Sauk JS, et al. Stress and Ulcerative Colitis Flares. Clin Gastroenterol Hepatol 2022.
LINEやWEBから、かんたんにご予約できます。
お好きな方法でお気軽にご予約ください。
※この記事は2022年9月8日に公開され、2025年4月29日に更新されました。
施設紹介
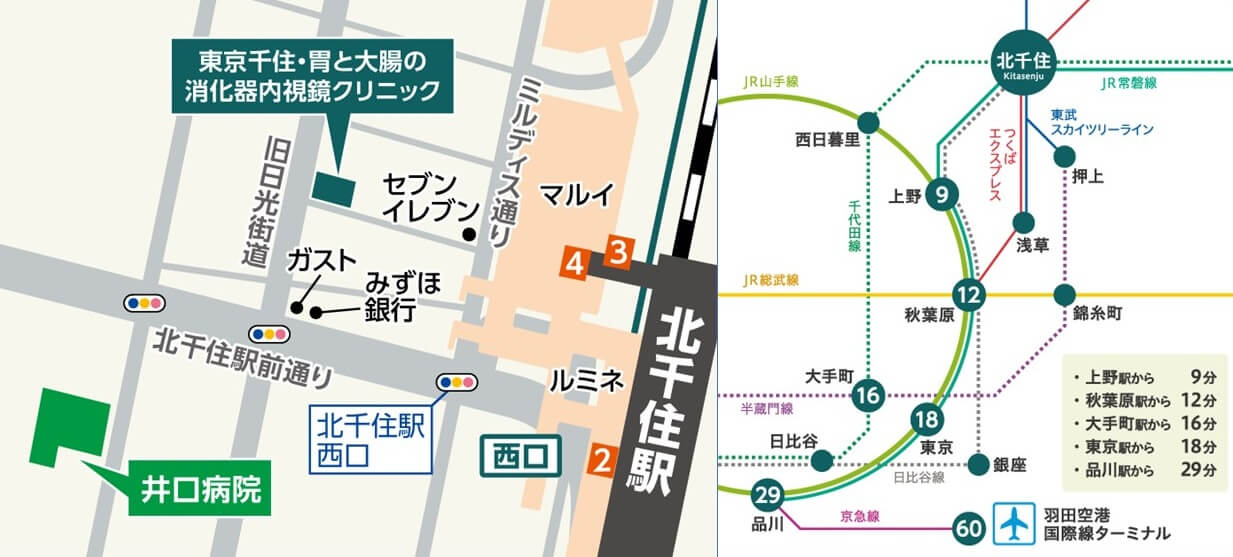
東京千住・胃と大腸の消化器内視鏡クリニック 足立区院 >>
ホームページ https://www.senju-ge.jp/
電話番号 03-3882-7149
住所 東京都足立区千住3-74 第2白亜ビル1階
| 診療時間 | 月 | 火 | 水 | 木 | 金 | 土 | 日 |
|---|---|---|---|---|---|---|---|
| 9:00~12:00 | ● | ● | ● | ● | ● | ● | ● |
| 14:00~17:30 | ● | ● | ● | ● | ● | ● | ※ |
※予約検査のみ
※祝日のみ休診
JR北千住駅西口より徒歩2分、つくばエクスプレス北千住駅より徒歩2分、東京メトロ日比谷線北千住駅より徒歩2分、東京メトロ千代田線北千住駅より徒歩2分、東武伊勢崎線北千住駅より徒歩3分